| |
Determinación de la máxima
capacidad de adsorción de la tierra
de Arriera en la eliminación de fosfatos
en soluciones acuosas
Determination of the maximum adsorption
capacity Arriera land in removing phosphates
in aqueous solutions
|
| |

Infografía:.
Proceso de adsorción utilizando tierra
de arriera en soluciones acuosas (aguas eutrofizadas).
|
*Recibido: 5 Noviembre
2013
|
*Aceptado: Noviembre
12 2013
|
Nivaldo E. Vargas
Soriano, Candidato Ph.D.
Universidad Politécnica de Cataluñya,España.
|
Lazaro V. Cremades.
Ph.D.
Profesor
Departamento de de Proyectos de Ingeniería,
Universidad Politécnica de Cataluñya,
España.
|
| vnivaldos@hotmail.es
|
|
Jose
Villareal, Ph.D.
Profesor
Departamento de Suelos y Aguas del Instituto de
Investigaciones Agropecuarias, Panamá.
|
Ditza
Medina, M.Sc.
Profesor
Departamento de Química.
Universidad de Panamá. Centro Regional de
Veraguas. |
|
|
|
Resumen
Los
materiales existentes en el trópico como es la
tierra de arriera pueden ser usados como una herramienta
de biorremediación en procesos de purificación
y descontaminación de aguas residuales contaminadas.
El objetivo de este estudio consistió en determinar
la máxima capacidad de adsorción de tierra
de arriera en la eliminación de fosfatos en periodos
de tiempos determinados. La metodología aplicada
consistió en la extracción de fósforo
adsorbido por las arcillas y la técnica de Melhich,
a fin de evaluar el fósforo adsorbido por la
arcillas en tiempos de adsorción, se utilizó
solución carolina del norte y se midieron la
concentraciones en un espectrofotómetro de UV
a longitudes de ondas de 680 nm. Las muestras evaluadas
fueron sometidas a tiempos de adsorción, donde
reflejan si son consistentes y aptas para la investigación.
Los resultados obtenidos demuestran que la tierra de
arriera, variando sus tiempos de adsorción, tienen
la capacidad de adsorber fosfato disponible en las soluciones
acuosas y la que respondió a una mayor eliminación
fue la muestra de Macaracas (M2) con un 79% de eliminación
de fosfato.
Palabras
Clave
Adsorción, tierra de arriera, fosfatos, soluciones
acuosas, eutrofización.
ABSTRACT
Existing materials in the tropics (land of Arriera),
can be a tool in bioremediation processes of purification
and decontamination, contaminated wastewater. The objective
is to determine the maximum adsorptive capacity of land
f in the elimination of phosphates in certain periods
of time. The methodology used has been the removal of
phosphorus in clays and the technique of Melhich, in
order to assess the phosphorous adsorbed by clay in
times of adsorption, use the solution of North Carolina
and measure concentrations in a spectrophotometer UV
to wavelengths of 680 nm. The samples were subjected
to adsorption times, where reflected be consistent and
suitable for the investigation- The results obtained
show that the land of has the capacity to adsorb phosphate
available in aqueous solutions by varying its adsortion
time. The sample that shower the greatestr adsorption
was the sample Macaracas (M2) with 79% of phosphate
removal.
Key Words
Adsorption, land of Arriera, phosphates, aqueous solutions
and eutrophication.
1. Introducción
En las zonas tropicales existe una gran variedad de
materiales que pueden ser utilizados para el desarrollo
de investigaciones científicas; tal es el caso
del material de suelo conocido como tierra de arriera.
Consiste en una arcilla que extrae la hormiga arriera
(Atta cephalote) de sus cuevas o galerías del
fondo del suelo, propia de los trópicos y cuyo
material es abundante y sin utilidad para la ciencia.
El
proceso de adsorción es conocido desde hace mucho
tiempo. Se cree que el término adsorción
fue introducido por primera vez por Kayser en 1881 para
describir sus observaciones sobre la condensación
de gases sobre una superficie (Canadell, 2010).
Dabrowski
(2001) plantea que el fenómeno fué descubierto
por Sheele, quien observó que el carbón
tomaba varias veces su propio volumen de aire y que
este fenómeno era reversible: al calentarse,
el aire se expulsaba del carbón, y al enfriarse
volvía a ser absorbido y también por parte
de Fontana en 1777 de forma independiente. En la actualidad,
la adsorción se conoce como un fenómeno
importante para la mayor parte de los procesos físicos,
naturales, biológicos y químicos.
Es
por tal razón, que la adsorción, es un
fenómeno superficial que puede ser definido como
el incremento de concentración de un determinado
componente a la superficie entre dos fases. Estas fases
pueden ser de las siguientes combinaciones: líquido-líquido,
líquido-sólido, gas-sólido, y gas-líquido.
En
la práctica, se entiende por adsorción
la eliminación de uno o más componentes
presentes en una fase líquida o gaseosa mediante
un sólido (Canadell, 2010). Pero se puede decir
que la adsorción se considera una de las reacciones
del fósforo, más estudiada en los suelos,
ya que controla la disponibilidad del mismo en la planta
(Sawal & Kumar, 1995; citado por Medina, 2003).
Puede verse que el movimiento del fósforo se
realiza principalmente por difusión y, en menor
grado, por flujos de masas (Sitio Agrícola, 2001).
El contenido total de fósforo depende de la textura
de los suelos: cuanto más fina es, mayor es el
contenido de fósforo. De igual manera, el contenido
total de fósforo varía con la profundidad
del suelo, lo que se explica por la disminución
de materia orgánica y por el avance de la meteorización
del perfil (Sawal & Kumar, 1995).
La fijación está determinada por la mineralogía
de las arcillas, la cantidad de arcilla, la cantidad
de coloides amorfos, el aluminio (Al) y el hierro (Fe)
intercambiable y la materia orgánica (Bertsch,
1995). La mayoría de los suelos tienen la capacidad
de adsorber y retener grandes cantidades de fosfatos
aplicados (Michael, 1998). Cuanto mayor es el porcentaje
de arcillas, mayor es la fijación de fósforo
y se ha encontrado que los suelos ultisoles poseen la
más alta capacidad de fijación de fósforo
(aluminosilicato no cristalizado) y de óxidos
de aluminio (Bertsch, 1995).
El fósforo en el suelo puede presentarse en forma
orgánica y en forma inorgánica. La mayor
parte del fósforo inorgánico se encuentra
en la fracción de las arcillas, en forma de fosfatos
de (calcio en suelos básicos y de hierro en suelos
ácidos) (Medina, 2003).
También se encuentra el fósforo en las
aguas superficiales y residuales casi exclusivamente
en forma de fosfatos (ortofosfatos, fosfatos condensados
y otros polifosfatos ligados orgánicamente).
Los ortofosfatos aplicados como fertilizantes a la tierra
cultivada agrícola son arrastrados a las aguas
superficiales por las lluvias (Romero, 2002).
El fósforo es un nutriente que en exceso promueve
el crecimiento de macro y microorganismos acuáticos,
los cuales se convierten en la principal causa de eutrofización
de los cuerpos receptores (Karacas et al., 2004; Namasivay
y Sanjeetha, 2004).
El problema de la eutrofización está ampliamente
estudiado; sin embargo, las últimas tendencias
internacionales en tratamiento de aguas dirigen la importancia
de este parámetro a la presencia de algas cianofíceas
que pueden generar problemas en los sistemas de potabilización
(Romero, 1996).
La
concentración de fosfatos en los cuerpos de aguas
superficiales representa un problema debido a la reproducción
en progresión geométrica de los organismos
unicelulares que dependen del fósforo como fuente
de alimentación (Romero, 1996).
Existen algunas técnicas para la eliminación
de fosfatos, tal es el caso de la utilización
de coagulantes con sulfato de aluminio y cloruro férrico
(Díaz et al., 2007).
En este estudio se utilizó un material presente
en el neo trópico, la tierra de arriera, producida
por la hormiga arriera Atta cephalotes, la cual se encuentra
mayormente distribuida desde México hasta el
sur de Brasil (Fernández y Sandoya, 2004).
La
remoción de tierra (Montoya et al., 2006) es
uno de los efectos notables causados por la colonización
de Atta en la aparición de nidos u hormigueros,
los cuales se distinguen por la presencia de montículos
de tierra suelta, producto de las excavaciones en el
suelo para construir subterráneamente sus nidos.
El
objetivo primordial de esta investigación consiste
en determinar la máxima capacidad adsortiva de
la tierra de arriera en la eliminación de fosfato,
en periodos determinados de tiempo, para soluciones
acuosas. Se desea conocer el grado de utilidad que se
le puede dar a este tipo de material como agente adsorbente
del ion fosfato, que es el causante de la contaminación
de las fuentes de aguas superficiales, mediante el proceso
de eutrofización en lagos, ríos, quebradas
y aguas estancadas, producto de las descargas de aguas
contaminadas en la fincas agropecuarias por el lavado
de porquerizas y lechería.
2. Materiales y Métodos
El material utilizado como adsorbente, la tierra de
arriera, existe en grandes cantidades en Panamá,
por lo que puede ser un instrumento natural para la
eliminación de fosfatos, producto de la contaminación
de aguas emanadas de fincas agropecuarias.
Este
tipo de arcilla se ha decidido estudiarla, a fin de
garantizar su utilidad, y determinar la capacidad de
adsorción que puedan tener del ion fosfato por
parte de estos materiales en tiempos determinados de
adsorción (1, 6, 12, 24 horas), y con una concentración
conocida de 5 mg/l en una disolución preparada
en laboratorio.
Muestras
Las
muestras de suelo de arriera fueron tomadas en diferentes
sitios de Panamá. Los sitios escogidos y sus
coordenadas geográficas fueron los siguientes:
Los Santos (Macaracas N 7° 41´ 13" y
O 80° 31´ 57") Herrera (Portobelillo
N 8° 02´ 01" y O 80° 34´ 03"),
y Veraguas (Calabacito N 8° 14´ 10" y
O 81° 04´ 40"). Además, se tomó
una muestra de mesocarpio del coco ( N 7° 41´
53" y O 80° 32´ 37"). Este último
es un material inorgánico, fibroso que recubre
el coco de agua y que podría servir como alternativa
a la tierra de arriera en cuanto a material adsorbente
de fosfato.
Se
tomó una muestra en cada sitio, sumando un total
de 5 muestras. Fueron recolectadas en cartuchos plásticos
transparentes de 1 kg de peso y se mantuvieron a temperatura
ambiente para su posterior análisis fisicoquímico,
donde se rotularon con nombres y procedencia (Idiap,
2009).
Materiales
Se
preparó una solución patrón de
fosfato (K2PO4), a concentración de 5 mg/l, para
realizar la corrida de los ensayos en tiempos determinados
(1, 6, 12, 24 horas).
Se
pesaron 2,5 gramos de suelo seco a temperatura ambiente
y se colocaron en frascos de 50 ml en duplicados, para
cada una de las muestras a analizar.
Para medir la concentración del fosfato adsorbido
o eliminado por la arcillas se utilizó un espectrofotómetro
serie Génesis 105 UV- Vis Thermo Scientific,
calibrado a 680 mn de lectura en adsorbencia.
Los
equipos de laboratorio utilizados fueron: un agitador
de jarras, cristalería (vasos químicos,
agitadores) una centrifugadora Universal Hettich Zentrifugen
de 5.000 rpm, una balanza digital y reactivos químicos
tales como, ácido ascórbico, molibdato
de amonio y solución de Carolina del Norte.
Método
El método utilizado para determinar la capacidad
de adsorción o eliminación del ion fosfato
por parte de la arcillas (tierras de arriera) fue el
Método de Carolina del Norte o prueba de Mehlich
(1984) para la determinación de fósforo
en suelos. Según Faca (2000), la prueba de Mehlich
es la más aceptable para evaluación del
fósforo presente en las arcillas de Panamá.
Cada
muestra se analizó por duplicado con las dosis
seleccionadas durante el tiempo establecido. Puesto
que se ensayaron 5 muestras en dobles repeticiones,
se le aplicó la corrida a los diferentes tiempos
de adsorción (4), por lo cual se tuvo un total
de 24 muestras analizadas.
Se
tomaron los 2,5 gramos de suelo y se les agregó
25 ml de solución sintética preparada
de 5 mg/l. Luego se agitaron durante 10 minutos y se
dejaron en reposo para los diferentes tiempos de adsorción
de 1, 6, 12, y 24 horas. Pasado el tiempo de reposo
se les retiró la solución de fosfato y
se les incorporó solución Carolina del
Norte, donde nuevamente las arcillas muestreadas fueron
agitadas y dejadas en reposo 10 minutos. Luego, fueron
centrifugadas para la extracción de la solución
líquida que sería analizada.
Una
vez terminada la extracción filtrante de la muestra,
se tomaron alícuotas de la solución resultante
(2,5 ml), y se le agregó 14,5 ml de solución
de ácido ascórbico más molibdato
de amonio. Se le dejó en reposo 30 minutos para
que adquiriera una coloración azulada, la cual
es utilizada para la determinación del ión
fosfato presente en las soluciones por el método
basado en un complejo fosfomolíbdico, usando
ácido ascórbico como reductor.
La intensidad de esta coloración azul se mide
mediante el uso del espectrofotómetro de luz
visible a una longitud de onda de 680 nm (Radojevic
& Bashkin, 1999).
3. Resultados y Discusiones
Los resultados obtenidos se presentan en la Tabla 1.
Las muestras evaluadas fueron: Santiago (M1), Macaracas
(M2), Portobelillo (M3) y Calabacito (M4) y Mesocarpio
del coco (M5), a las cuales se les extrajo el fósforo
disponible presente.
Tabla
1 Resultados de evaluación de fósforo
disponible en las arcillas y en el mesocarpio coco
.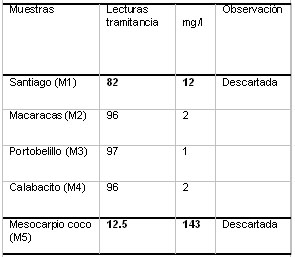
De la Tabla 1, se destaca que el mesocarpio del coco
tiene una disponibilidad presente de 143 mg/l de fósforo.
Se realizó una depuración de las muestras
con altas concentraciones de fósforo en su estructura
y que no ayudarían al desarrollo de la investigación,
como fueron: Santiago (M1) y mesocarpio de coco (M5).
Estas muestras fueron descartadas ya que los parámetros
permitidos por la norma panameña admiten valores
de
fósforos totales hasta 5 mg/l para vertidos a
efluentes superficiales (COPANIT- 35-2000).
Tabla
2 Resultados de capacidad de eliminación de fosfato
por las arcillas en tiempos determinados.
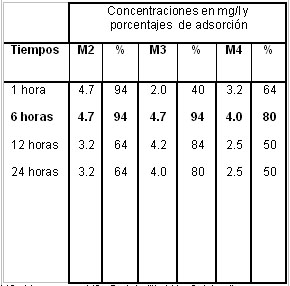
Las muestras de Macaracas, Portobelillo y Calabacito
presentaron la menor disponibilidad de fósforo
presente en su estructura, lo que ha permitido utilizarlas
para
la eliminación de fosfato en soluciones.
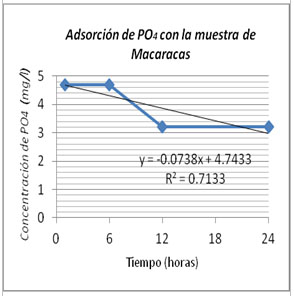
Figura
2 Eliminación de fosfato en la muestra de Macaracas
a lo largo del tiempo.
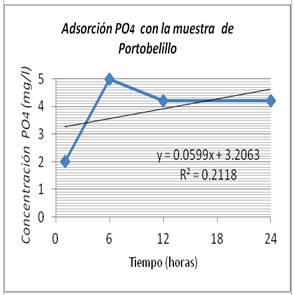
Figura
3 Eliminación de fosfato en la muestra de Portobelillo
a lo largo del tiempo.
En
la Tabla 2 se indica la capacidad de adsorción
o eliminación de fosfato en periodos de tiempos
determinados por parte de las arcillas evaluadas.
Los resultados obtenidos demuestran que el periodo de
6 horas de adsorción o eliminación de
fosfato por parte de las muestras evaluadas (M2, M3
y M4) es el que arroja los mejores resultados. Entre
las tres tierras de arrieras ensayadas, la muestra de
Macaracas es la que permite mayores porcentajes de adsorción.
Las Figuras 2, 3 y 4 muestran la variación de
la capacidad de eliminación de fosfatos para
los diferentes tiempos seleccionados en cada una de
las muestras analizadas.
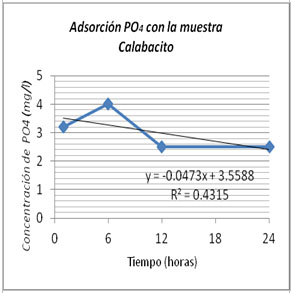
Figura
4 Eliminación de fosfato con la muestra de Calabacito
a lo largo del tiempo.
5.
Conclusiones
Esta investigación ha probado que las tierras
de arrieras estudiadas podrían ser utilizadas
para procesos de eliminación de fosfatos en aguas
contaminadas provenientes de las actividades agropecuarias.
La
muestra del sitio de Macaracas (M2), produjo el mayor
grado de adsorción o eliminación de fosfatos,
presentes en la solución acuosa propuesta de
5 mg/l, con valores promedio de adsorción de
79 %.
4. Referencias Bibliográficas
Bertsch, F. (1995). La fertilidad de los suelos y
su manejo. Asociación Costarricense de la Ciencias
del Suelo. Costa Rica.
Canadell, A. E. (2010). Comparación de la adsorción
del boro en perlas de alginato y alginato/alúmina.
Proyecto final de Carrera. Ingeniería Química.
Universidad Politécnica de Catalunya. España.
Pág. 58-59.
Dabrowski,
K. (2010). Ascorbic Acid in Aquatic Organisms: Status
and Perspectives. Boca Raton, FL; CRC Press.
Díaz, H.; Wilson; M.; Gonzaga Balmes, L. y
Contreras, N. (2007). Determinación del Coagulante
que Permita la Máxima Remoción de Fosfatos
en Agua Cruda del Río Otún. Scientia
Et Technical, Mayo, año/vol. XIII. Número
034. Universidad Tecnológica de Pereira. ISBN
(versión Impresa): 0122-1701. Colombia. pp.
607-612
El Sitio Agrícola (2001). Movilidad del fósforo
en el Suelo. http://www.elsitioagricola.com/art.../Movilidad
del fósforo en le suelo.as, 10 de Octubre 2001.
Fernández, F. y Sandoya, S. (2004). Lista de
la hormigas Neotropicales. (Hymenoptera: Formicidae).
Biota Colombiana 5(1): 3-93
Instituto de Investigaciones Agropecuarias (IDIAP)
(2009). El Muestreo de suelos para análisis
de fertilidad. Manual elaborado por: Agudo, Lwonel,
Villalaz, Jhon, Villarreal, José. Panamá.
Karaca, A. ; Gurses ,M.; Edjer, M.; Acikyildiz, J.
(2004). Colloid Interface Sci. 277. pp 257-263.
Medina, D. (2003). Estudio de Fósforo en un
Ultisol en Sistema de Fríjol Tapado. Tesis
de Maestría en Química. Universidad
de Costa Rica. Rodrigo Facio. Costa Rica. Pág.
4.
Mehlich,
A. (1984). Soil Test Extractant: A modification of
Melhich II Extratante. Commun. Soil Sci. Plant Anal.
15(12): 1409-1416.
Michael,
R.& et, al. (1998). Manual de Agronomía.
Análisis de suelos y Plantas. Laboratorio Agrícola
A&L. Mexico. pp. 132.
Ministerio
de Comercio e Industrias (2000). Normas de Calidad
de Aguas. Descarga de efluentes líquidos directamente
a cuerpo y masas de aguas superficiales y subterráneas.
DGNTI- COPANIT 35-2000. Panamá. Pág.
32.
Montoya, J. L; Chacón, P. y Manzano. M. (2006).
Caracterización de nidos de la hormiga arriera
Attacephalotes (Hymenoptera: Myrmicinae) en Cali (Colombia).
Revista Colombiana de Entomología 32(2): 151-
158
Namasivayam,
D. and Sangeeth, J, (2004). Colloid Interface Sci.
280. pp 359-365.
Radojevic,
M. and Bashkin, V. N. (1999). Practical Enviromental
Analysis, MPG Books Ltd., Cornwal, England.
Romero. R. y Jairo A. (2002). Calidad del Agua. Editorial
Escuela Colombiana de Ingeniería. 1ra Edición,
Bogotá. Colombia.
Romero, R. y Jairo, A. (1996). Acuaquimica. Escuela
Colombiana de Ingeniería. Editorial Presencia,
1ra Edición, Bogotá. Colombia.
Sawal, O. and Kumar, V. (1995). Común. SoilSci.
Plant anal. 26: 3181-3192.
Vaughgan,
D. and Malcolm, R. E. (1985). Soil organic and biological
activity. The Institute for Siol Research. Martinus
Nijhff/Dr. W. Junk. Publisher. Scotland.
|

